Nucleofil
În acest articol vom explora viața fascinantă a lui Nucleofil, un personaj care și-a pus amprenta în istoria umanității. De la realizările sale incredibile până la provocările și obstacolele sale, ne vom lansa într-o călătorie prin moștenirea sa, în care vom descoperi cele mai relevante aspecte ale carierei sale. În acest sens, vom explora impactul său asupra societății, contribuțiile sale la lume și moștenirea pe care a lăsat-o generațiilor viitoare. Pregătește-te să te cufunzi în povestea captivantă a lui Nucleofil și să descoperi ce îl face atât de special.
Un nucleofil este o specie chimică (un ion sau o moleculă) care poate să cedeze electroni sau perechi de electroni unui electrofil pentru a forma o legătură chimică. De exemplu, bazele Lewis sunt nucleofili, dar și ionii negativi, precum ionul clorură Cl-, și moleculele neutre cu perechi de electroni libere, precum amoniacul (NH3), aminele (R-NH2), apa (H2O) și alcoolii (R-OH).[1]
Proprietăți
Reacții chimice
Substituția nucleofilă
Are loc o reacție de substituție al unui atom sau grupare de atomi cu o specie nucleofilă. Avem ca exemplu reacția unei halogenuri de alchil primare cu un ion hidroxil:
Adiția nucleofilă
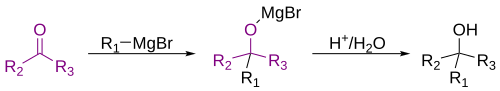
Are loc o reacție de adiție a speciei nucleofile la gruparea electrofilă. Avem ca exemplu reacția compușilor organomagnezieni (reactivi Grignard) cu cetonele:
Tipuri
Halogen
Halogenii ca atare nu sunt specii nucleofile, însă anionii lor sunt specii nucleofile bune. În solvenți polari protici, F− este cel mai slab nucleofil, iar I− este cel mai puternic. Ordinea se inversează în solvenți polari aprotici.[2]
Azot
Azot-nucleofilii sunt: amoniacul, aminele, azidele, hidroxilaminele, hidrazinele, fenilhidrazinele, carbazidele, semicarbazidele și amidele.[3][4]
Carbon
Carbon-nucleofilii sunt adesea compuși organometalici, exemple fiind: reactivi Grignard, compușii din reacțiile Reformatsky, Barbier, compușii organolitici (N-butillitiu) și acetilurile.[5]
Alte exemple includ enolii (implicați în reacții de condensare aldolică și condensare Claisen), cianurile, nitrilii și fosforilidele.[5]
Oxigen
Oxigen-nucleofilii sunt: apa, alcoolii, anionul hidroxid și anionii alcoxid, peroxidul de hidrogen.[6] În urma reacției dintre aceștia și compuși carbonilici se formează hidrați (cu apa), hemiacetali și acetali (cu alcooli).[6]
Sulf
Sulf-nucleofilii sunt: hidrogenul sulfurat, sulfurile, tiolii, anionul tiolat și ditiocarbamații.[7]
Vezi și
Referințe
- ^ Dicționar de chimie John Daintith, traducere de Mihaela Rudeanu și Lia Cojocaru; ediția a VI-a, Editura All, 2010, București; pag. 339, ISBN 978-973-684-725-7
- ^ „Nucleophile”, Chemistry LibreTexts, , accesat în
- ^ „Reaction of Aldehydes and Ketones with Nitrogen Nucleophiles”, Chemistry LibreTexts, , accesat în
- ^ „Nitrogen Nucleophiles - Course Hero”, Coursehero.com, accesat în
- ^ a b „Carbon Nucleophiles - Course Hero”, Coursehero.com, accesat în
- ^ a b „Oxygen Nucleophiles - Course Hero”, Coursehero.com, accesat în
- ^ „Nucleophilicity of Sulfur Compounds”, Chemistry LibreTexts, , accesat în