Porfirină
În acest articol, vom explora în continuare subiectul Porfirină, care a captat atenția experților și entuziaștilor deopotrivă în ultimii ani. De la origini și până la impactul asupra societății de astăzi, prin aplicațiile sale practice și relevanța în diverse domenii, Porfirină a devenit un subiect de interes din ce în ce mai mare în domeniul academic și profesional. Prin această analiză exhaustivă, ne propunem să facem lumină asupra diferitelor aspecte ale Porfirină, oferind o viziune completă și actualizată asupra importanței și influenței sale în lumea contemporană.
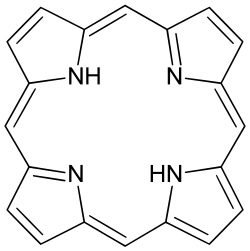

Porfirinele reprezintă un grup de compuși organici heterociclici macrociclici, alcătuiți din patru subunități pirolice interconectate la atomii de carbon α prin punți metin (=CH−). Cea mai simplă porfirină este porfina, iar restul porfirinelor sunt substituite. Nucleul porfirinic (cum este adesea denumit) are o structură aromatică, având un total de 26 de electroni în sistemul conjugat. Diferite analize au indicat faptul că nu toți atomii din structura nucleului porfirinic sunt implicați în mod egal în conjugare, sau că natura moleculei s-ar putea baza pe mai multe sisteme conjugate mai mici.[1][2]
Porfirinele sunt de obicei intens colorate; numele de „porfirină” provine din limba greacă, unde πορφύρα (porphyra) înseamnă violet.[3] Multe porfirine sunt răspândite în natură, precum hemul (compus extrem de important ce intră în structura hemoglobinei) și clorofila.
Complecși ai porfirinelor
Porfirinele sunt acizii conjugați ai liganzilor care leagă metale pentru a forma complecși. Ionul metalic are de obicei sarcina 2+ sau 3+. O ecuație schematică pentru o reacție de sinteză a complecșilor porfirinici este următoarea:
- H2porfirină + 2+ → M(porfirinat)Ln−4 + 4 L + 2 H+
- unde M = ionul metalic, iar L = un ligand
O porfirină fără ion metalic complexat este o bază liberă. Complecșii metalici ai porfirinelor sunt adesea întâlniți în natură; avem astfel hemul și hemoproteinele (complecși cu fier), hemoglobina și mioglobina (proteine care leagă oxigen și conțin porfirine cu fier), citrocromi, clorofila (conține ion de magneziu), etc.
Sinteză
Aplicații
Vezi și
Referințe
- ^ Ivanov, Alexander S.; Boldyrev, Alexander I. (). „Deciphering aromaticity in porphyrinoids via adaptive natural density partitioning”. Organic & Biomolecular Chemistry. 12: 6145–6150. doi:10.1039/C4OB01018C.
- ^ Lash, Timothy D. (). „Origin of aromatic character in porphyrinoid systems”. Journal of Porphyrins Phthalocyanines. 15: 1093–1115. doi:10.1142/S1088424611004063.
- ^ Harper, Douglas; Buglione, Drew Carey. „porphyria (n.)”. The Online Etymology Dictionary. Accesat în .